最新!又有7個藥通過一致性評價,大洗牌來了來源:賽柏藍網址:http://news.PharmNet.com.cn
9月10日訊 終于來了! 未通過一致性評價藥品,淘汰!通過一致性評價藥品,勝利在望! ▍又有7個藥品通過一致性評價 9月10,哈爾濱三聯藥業發布公告,稱公司產品米氮平片(15mg)已通過一致性評價,為國內首家通過該品種一致性評價。  據悉,米氮平片為哈爾濱三聯藥業的主要產品之一。截至目前,公司在米氮平片一致性評價項目上已投入研發費用約735萬元人民幣。 此外,近日賽柏藍查詢《中國上市藥品目錄集》發現,又有6個品種被納入目錄集,根據相關政策規定,視同通過一致性評價。 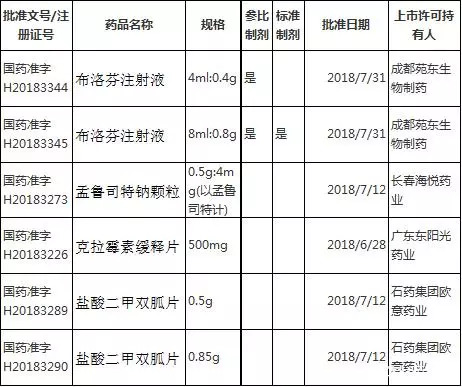 據業內人士透露,國家醫保局牽頭的11城市聯合集中帶量采購方案,馬上就要出臺了。而這個采購方案,就是主要針對目前的通過一致性評價藥品的。 方案提出,“不分質量層次,唯一中標,60-70%市場份額”的思路,會讓通過一致性評價藥品在市場占有率和增長率方面,有一個極大的飛躍。 業內專家表示,一旦該方案實施,醫保會節省上百億資金,外企原研藥會損失上百億市場,而國內通過一致性藥品,在銷量上將會有極大幅度增長的潛力。 ▍大批仿制藥將被踢出市場 近日,北京醫藥集中采購信息網發布《關于陽光采購藥品數據庫實行動態調整的通知》,明確將實行動態調整,產品有進有出,將按照合規產品納入、休眠產品下架、雙方按需激活原則建立相應目錄,在此基礎上實施采購。  通知要求,對于國家抗癌藥政策所涉藥品、通過質量和療效一致性評價所涉藥品等,開放綠色通道,加快準入。 一致性評價,近日以來,可謂是牽動著千萬醫藥人的神經。 根據2016年3月5日,國務院辦公廳印發的《關于開展仿制藥質量和療效一致性評價的意見(國辦發〔2016〕8號)》,明確要求,同品種藥品通過一致性評價的生產企業達到3家以上的,在藥品集中采購等方面不再選用未通過一致性評價的品種。 隨著通過一致性評價的品種越來越多,目前,不少地區已開始落實上述政策,這也是大家重點關注的。 近日,江西省醫藥采購服務平臺連發兩則通告,由于部分產品通過一致性評價的已經集齊3家,有6家企業的6個產品被暫停掛網、不允許參加網上采購。 先后暫停了山東仙河藥業的“蒙脫石散3g”、安徽貝克生物的“富馬酸替諾福韋二吡呋酯片300mg”、康普藥業股份、浙江京新藥業股份有限公司、輔仁藥業集團有限公司、北京紅林制藥有限公司的“苯磺酸氨氯地平片5mg”的網上采購資格。 此外,據賽柏藍統計,截至目前為止,浙江、廣西、福建、天津、河北、吉林、遼寧、陜西、甘肅等多省市,也已發文對同品種通過一致性評價的企業達3家以上的,暫停采購未通過一致性評價的品種,進行明確規定。 ▍一致性評價,大限將至 大家都知道,目前國家藥品監督管理局已經公布的5批通過一致性評價的藥品名單中,“289品種”只有13個(24個品規),加上《中國上市藥品目錄集》更新的視同通過一致性評價的品種,也遠遠達不到國家的要求。 就目前通過的數量來看,國務院《關于開展仿制藥質量和療效一致性評價的意見》中給的“2018年年底”的大限,行業普遍的預期是要推遲。否則,大限將至,會有大批289目錄中未過一致性評價的藥品被淘汰。 9月4日,上海市食藥監局發布《上海市食品藥品監督管理局關于深化“放管服”改革優化行政審批的實施意見》,明確規定,“對國家基本藥物目錄中口服制劑未通過一致性評價的不予再注冊”,“對國家基本藥物中口服固體制劑不符合要求的藥品予以淘汰”。 距離“大限”只有4個月了,時間極為緊迫。 然而,從上海文件的字里行間,我們可以感受到,雖然距離“大限”越來越近,但“大限”的要求仍不會更改。不僅上海,近日黑龍江、江蘇等省也相繼發文,明確“大限”要求。 9月4日,黑龍江人民政府發布了《關于改革完善仿制藥供應保障及使用政策的實施意見》,明確指出,將嚴格執行國家規定,對在規定期限內未通過一致性評價的仿制藥不予再注冊。 8月27日,江蘇省辦公廳發布的《關于改革完善仿制藥供應保障及使用政策的實施意見》提到,“指導企業按照國家政策和時限要求開展已上市仿制藥一致性評價工作”,在這一段文字中,“時限”二字被重點強調,這無疑在刻意提醒企業,年底“大限”將至,不可忽略。 事實上,自今年4月,國務院發布《關于改革完善仿制藥供應保障及使用政策的意見》后,江蘇、黑龍江、遼寧、天津、陜西、甘肅等十多個省市已相繼發布相關文件,要求藥企加快仿制藥一致性評價工作。 總的來看,無論一致性評價時間大限是否會推遲,所有在289個基藥范圍內的品種,都已經進入生死倒計時。 接下來的最后幾個月,相信會有更多藥品扎堆通過一致性評價。而那些無法按時通過一致性評價的品種,也將迎來更加猛烈的行業洗牌。
|


